Avastin-Lucentis: quando un farmaco può letteralmente costare un occhio
Tra insicurezze dei medici e budget limitati degli ospedali, ai pazienti resta il dubbio di aver pagato con la propria vista i guadagni milionari delle farmaceutiche
Altri sviluppi
Avastin-Lucentis: il caso
Vedi anche: Avastin-Lucentis: la testimonianza
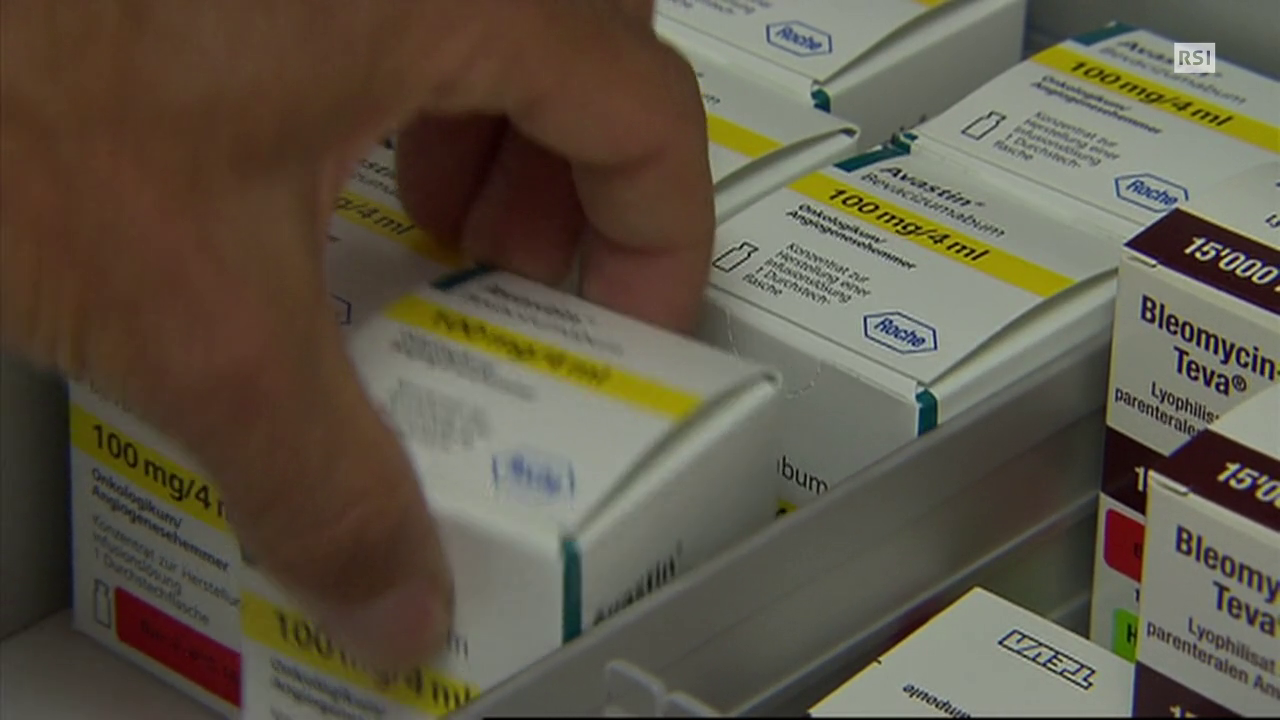
La multa comminata dall’Antitrust italiano ha un significato circoscritto al mercato: i gruppi svizzeri Roche e Novartis, secondo l’Autorità garante, hanno artificiosamente differenziatoCollegamento esterno i farmaci Avastin (bevacizumab) e Lucentis (ranibizumab) per ostacolare la diffusione del prodotto più economico, causando al Servizio sanitario nazionale una maggiore spesa fino a oltre 600 milioni di euro l’anno.
Ma per quale ragione questa intesa avrebbe minato la salute dei pazienti? Avastin, per quanto non sia più a carico dello Stato se usato per gli occhi, ha un prezzo accessibile ai pazienti stessi. Lucentis è caro ma è rimborsato. A prima vista vi è addirittura doppia possibilità di cura.
Intervistato da tvsvizzera.it, il presidente della Società oftalmologica italiana (Soi) Matteo Piovella parla di informazioni fuorvianti e budget limitati.
Da una parte, un’informativa dell’Agenzia italiana del farmacoCollegamento esterno (Aifa) avrebbe instillato il dubbio che Avastin fosse pericoloso, e il fatto che negli ospedali, oltre all’assunzione di responsabilità del medico oculista, sia necessaria la controfirma del direttore sanitario (di per sé una giusta tutela) avrebbe raddoppiato le incertezze e messo fuori gioco il prodotto meno caro. Dall’altra, l’informativa dell’Aifa è arrivata a fine anno, e i budget limitati delle strutture sanitarie non hanno permesso l’acquisto immediato di Lucentis.
In attesa di cure
Lidia Buccianti, portavoce di “Per vedere fatti vedere OnlusCollegamento esterno“, riferisce che in realtà alcune persone sono in lista d’attesa ancora oggi, per le iniezioni con il ‘nuovo’ farmaco. L’associazione – che organizza campagne a tutela della vista e dà sostegno pratico e psicologico ai pazienti – ha ricevuto dalla fine del 2012 qualche decina di richieste d’aiuto. La Società oftalmologica italiana stima intanto in decine di migliaia, le persone che non hanno ricevuto cure adeguate.
Saranno comunque le Procure a valutare la portata dell’evento, perché si possa stabilire se è stato disastro (è tra le ipotesi di reato nei fascicoli aperti a Torino e Roma) e se Roche e Novartis ne hanno colpa.
Per chi si è visto negare le iniezioni, la multa inflitta dall’Autorità garante della concorrenza e del mercato ha più che altro il merito di aver portato alla luce la vicenda. Non restituirà la vista a chi, come il signor Fea, è ormai sceso sotto la soglia della curabilità [ascolta la testimonianza della figlia].
Non si può dire con assoluta certezza come vedrebbe oggi il signor Fea, se la terapia fosse proseguita senza intralcio. Ma rimane il dubbio, a questa e altre famiglie che nelle ultime settimane hanno raccontato le loro storie sui giornali, di aver pagato con la propria salute le intese milionarie di aziende multinazionali.
Tra rimborsabilità ed efficacia
Nell’ottobre del 2012, la Commissione Tecnico Scientifica dell’Agenzia italiana del farmaco (Aifa) dispose la rimozione di AvastinCollegamento esterno dalla lista farmaci rimborsati dal Servizio sanitario nazionale anche quando usati in modalità non indicata dal produttore (off-label) ma inclusi in uno specifico elenco (chiamato 648/96Collegamento esterno, dalla legge cui fa riferimento).
Nella fattispecie Avastin, che Roche ha registrato per la cura del cancro, è impiegato in molti paesi anche attraverso iniezioni intravitreali (anziché endovenose) per curare alcune patologie della vista. Tanto che la stessa Aifa, nel 2007, ne aveva riconosciuto i beneficiCollegamento esterno.
In anni recenti, i National Institutes of Health statunitensi – constatata la diffusione dell’impiego off label – hanno commissionato uno studio dal quale è emerso che Avastin e Lucentis sono equivalenti nella cura della degenerazione maculare senileCollegamento esterno, nonostante una leggera differenza nell’insorgere di effetti collaterali. L’Organizzazione mondiale della sanità ha incluso Avastin nella sua Lista dei farmaci essenzialiCollegamento esterno, proprio per uso oftalmico.
Il cambio di rotta
Aifa giustifica il suo provvedimento dell’ottobre 2012 con un aggiornamento del “Riassunto delle caratteristiche del prodotto” operato dall’Agenzia europea del farmaco (Ema). Nella nuova versione del foglietto approvata dall’Ema, viene controindicato un uso intravitreale di Avastin.
Gli effetti avversi descritti, tuttavia, sono correlati alla modalità di somministrazione intravitreale in sé, e non all’anticorpo monoclonale alla base del farmaco. Quanto al capoverso “Effetti sistemici in seguito a somministrazione intravitreale”, esso è identico a quanto figura nel descrittivo di LucentisCollegamento esterno.
“Sono farmaci diversi”
Novartis, di recente, ha acquistato un’intera pagina pubblicitaria sui principali quotidiani italiani per spiegare al pubblico che Avastin e Lucentis “sono medicinali differenti”. La frase riassume l’unica posizione assunta finora dalle due aziende farmaceutiche, che hanno assicurato massima collaborazione con le autorità per chiarire i fatti e difendere la loro reputazione.
I due prodotti, prosegue il comunicato, “sono diversi tra loro per struttura e caratteristiche biologiche e derivano da processi produttivi differenti”, “la molecola Lucentis è stata progettata per essere iniettata nell’occhio” e il suo profilo di efficacia ampiamente studiato. Asserzioni che nessuno, a dire il vero, ha mai contestato.
“Al contrario”, si legge inoltre nella presa di posizione di Novartis, “Avastin è stato sviluppato e approvato esclusivamente per la somministrazione mediante infusione endovenosa e per il trattamento di patologie tumorali”. In realtà, ciò non significa necessariamente che se Roche avesse chiesto l’approvazione per uso intravitreale, questa sarebbe stata negata. Ma non l’ha chiesta: è un suo diritto.
Secondo l’Antitrust, Roche ha interesse a non ostacolare le vendite di Lucentis, perché attraverso la sua controllata Genentech – che peraltro ha sviluppato entrambi i farmaci – “ottiene su di esse rilevanti royalties da Novartis. Quest’ultima, dal canto suo, oltre a guadagnare dall’incremento delle vendite, detiene una rilevante partecipazione in Roche, superiore al 30%”.
La nostra richiesta di intervista a Roche Italia non ha avuto riscontro. Novartis ha invece declinato l’invito.
Rino Scarcelli

In conformità con gli standard di JTI
Altri sviluppi: SWI swissinfo.ch certificato dalla Journalism Trust Initiative




Se volete segnalare errori fattuali, inviateci un’e-mail all’indirizzo tvsvizzera@swissinfo.ch.